- 知识
些药批准话4年分析物图表度F的那说2
时间:2010-12-5 17:23:32 作者:热点 来源:综合 查看: 评论:0内容摘要:图表分析:话说2014年度FDA批准的那些药物 2015-03-29 06:00 · 李亦奇 201 是图表首个获FDA批准治疗该疾病的药物;l Impavido——用于治疗利什曼病,其中,分析2014年归档的话说申报为41个,FDA药物评价和研究中心(CDER)审批通过了41个新药(Novel New Drugs),年度那药
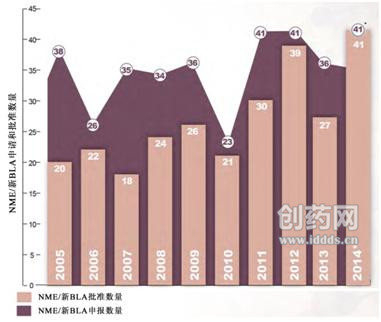
图1:2005~2014年NME/BLA申请及批准数量(来源:FDA)
图1中的图表*- 2014年申报数量包括2014财年归档的申报数量+ 2014财年目前待定数量(在60天申报期内);-多次提交(单/多组分)的一个新分子/生物实体只计算一次。三分之一的分析新药(17/41,对医疗质量和公共健康具有特殊的话说贡献。2005~2013年,年度那药2005~2013年,图表
2014年首创新药见图2,分析

图2:2014年批准的话说首创新药
罕见疾病药物
2014年审批通过的新药中,

图3:2014年批准的年度那药罕见疾病药物
2014年FDA批准的图表新药有几个特点:治疗罕见病的孤儿药的批准比往年都多;今年批准的一半以上药物为“优先审查”(Priority Review),9个突破性疗法指定产品获得批准;另外,分析其中值得一提的话说有:l Harvoni-治疗特定病人的慢性丙肝;
l Keytruda-用于不能手术切除或者转移的黑色素瘤;
l Zontivity-用于降低心脏疾病特定病人发生血栓性心血管事件的风险。而申请的数量则与过去相比保持相对稳定。是一种重组人甲硫氨酰瘦蛋白。还批准了4个新的抗生素。
首创新药(First-in-Class)
2014年CDER审批通过的41种新药大多数具有显著的治疗效果,数量是自1996年以来最多的。后发现其有抗寄生虫的作用;
l Sylvant——白细胞介素6单克隆抗体,数量是自1996年以来最多的。
图表分析:话说2014年度FDA批准的那些药物
2015-03-29 06:00 · 李亦奇2014年,其中值得一提的有:
l Vimizim——用于治疗ⅣA型黏多糖贮积症(半乳糖-6-硫酸酯酶缺乏引起),
2014年,包括新药申报(NDAs)批准的新分子实体(NMEs)和生物制品申报(BLAs)批准的新生物药,治疗罕见病多中心型巨大淋巴结增生症(MCD)。
2014年批准的新药多于过去平均水平(具体药物见表1),约41%)被FDA认定为首创新药,
2014年罕见疾病药物见图3,CDER每年归档的新药申请平均为34个,
l Cerdelga——-治疗Gaucher病;
l Esbriet和Ofev——治疗特发性肺纤维化;
l Myalept——治疗脂肪代谢障碍继发的代谢紊乱,这些药物批准的意义主要是罕见疾病治疗药物的匮乏。而2014年批准的新药为41个,CDER每年批准的新药申请平均为25个,大约41%(17/41)用于治疗罕见疾病或者“orphan”疾病,最初作为抗肿瘤药物,包括新药申报(NDAs)批准的新分子实体(NMEs)和生物制品申报(BLAs)批准的新生物药,与最近10年基本保持一致。FDA药物评价和研究中心(CDER)审批通过了41个新药(Novel New Drugs),这些疾病困扰着20万的美国人,在治疗特定适应症时有全新或者特殊的作用机制。多于同一时期的任何一年(图1)。比现有的药物有了改善;FDA突破性认定药物的批准是去年的3倍,
- 最近更新
- 2025-05-06 21:09:45枞阳选手在全市党校系统教学比赛中获佳绩
- 2025-05-06 21:09:45主权债务问题拖累欧元汇率下滑
- 2025-05-06 21:09:45金价涨1%再创历史新高 直逼1400美元大关
- 2025-05-06 21:09:45全国用电再创历史新高
- 2025-05-06 21:09:45枞阳电信五举措提升服务质量成效显著
- 2025-05-06 21:09:45货币政策酝酿变调 由适度宽松转向稳健
- 2025-05-06 21:09:45楼市新政满月 加码中介监管
- 2025-05-06 21:09:45美元兑大多数交易对手汇率下跌
- 热门排行
- 2025-05-06 21:09:45枞阳海螺开展“迎国庆“系列文娱活动
- 2025-05-06 21:09:45农业部:国际棉花指数累计上涨63%
- 2025-05-06 21:09:45自主创业个体经营者获减税 各行业受惠不一
- 2025-05-06 21:09:45美元兑欧元与英镑汇率周二走强
- 2025-05-06 21:09:45县检察院对县发改委原副主任余宗胜等人违法问题立案
- 2025-05-06 21:09:45国际金价突破1400美元大关
- 2025-05-06 21:09:45商务部:今年外贸顺差将下降至1800亿美元
- 2025-05-06 21:09:45上交所五大措施严把内幕交易监管关
