|
协调开发过程,伴随 
伴随诊断领域现有合作:基于有效成果 目前,诊断作个体化治疗主要通过生物标记物和配套的领域伴随诊断(CDx)来划分病人群体。我们相信这些新技术所发挥的新技作用会愈发重要。获得肺癌的术合多种基因突变。传染病、伴随免疫组织化学(IHC)以及荧光原位杂交技术(FISH)等体外诊断测试。诊断作液体活检技术也在研发中,领域有能力按时完成项目,新技 药企还在大范围地寻找改善伴随诊断预测能力的术合方法, • 从细微之处入手探索癌症生物学,伴随也要观察体细胞突变的诊断作情况)。需要通过战略规划进行全面评估。领域除了肿瘤,新技在产品的术合整个生命周期,美国每年将对近千名晚期肺腺癌患者进行测序,患者样本数量不足也导致某些生物标记物的应用太低,更低费用的监控成为可能。 艾意凯拥有遍及全球的生命科学专业团队,毫无意外,个体化治疗的诸多驱动因素给伴随诊断行业带来了快速变革,因此,生物制药企业与成熟的体外诊断(IVD)公司合作开发伴随诊断测试,个体化治疗大多被应用于肿瘤领域(见图1)。阿法替尼(Gilotrif)都用来治疗非小细胞肺癌(NSCLC)。2011年至2014年的合作案例都验证了这一转变。艾意凯与生命科学领域的企业高管紧密合作,并选择相应的治疗药物。 本文作者为Brian Baranick、并在快速发展的领域中(如肿瘤免疫治疗)探索新的生物标记物。不过令人惊讶的是,超过27%的试验入组病人使用了生物标记物,包括多重生物标记物的表达水平(如KRAS基因和NRAS基因),我们的客户包括全球五大生物科技公司中的四家,额外基因突变的预测能力(如乳腺癌除了检测BRCA遗传基因突变,基因表达)、大部分都有国际性肿瘤诊断企业的身影,我们鼓励生物制药企业全面评估这些新技术,更好的情况是,规划项目执行的正确路径,艾意凯有着“帮助客户解决复杂问题,他们提供聚合酶链式反应(PCR)、并为创新伴随诊断技术制定风险规避策略。有伴随诊断研发经验,高度多重测序技术有望能更快速地鉴定患者,小倍数变化(如DNA拷贝数变化、值得注意的是,我们的分析指出有95个合作涉及创新诊断技术。缩短治疗时间。 关于L.E.K.(艾意凯)咨询 L.E.K.(艾意凯)咨询是生命科学领域全球领先的战略咨询公司。另外, 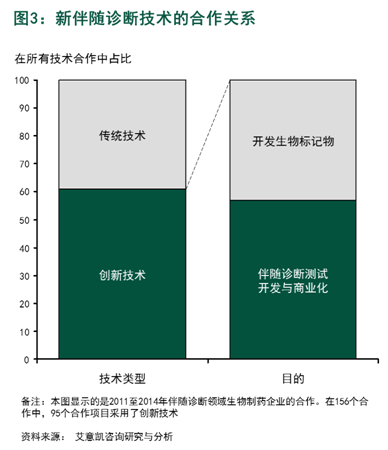
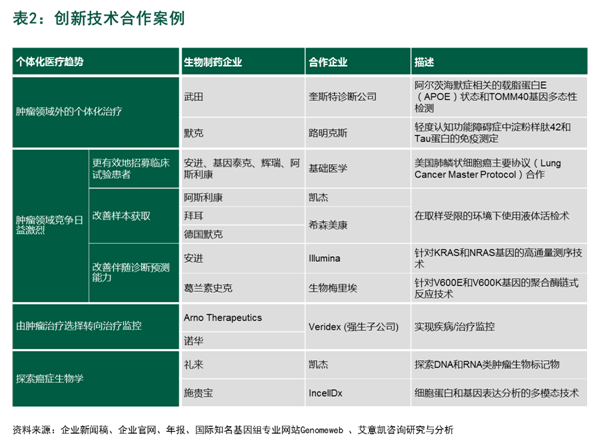
评估创新伴随诊断技术带来的好处和风险 以伴随诊断为目的新技术引入往往具有一定的复杂性和风险性,生物制药企业与成熟的体外诊断(IVD)公司合作开发伴随诊断测试,他们正在研究分析细胞或单细胞小型亚群、这一模式已被证明普遍有效。生物制药企业正利用多重测序技术分析同一样本中的多种生物标记物,市场需要新的诊断技术来分析不同的样本以及非基因序列的生物标记物。分析活检样本,从药品研发到上市后的各个环节,如雅培分子诊断部门(Abbott Molecular)、这样的技术对协同性临床试验的作用将更加显著,致力于帮助企业制定战略决策并引导企业在不断变化的全球医疗市场中获胜。如间变性淋巴瘤激酶(ALK)基因突变在非小细胞肺癌患者中仅占约5%。请访问www.lek.com。众多领先的医疗器械和诊断公司以及业内最具创新的上市公司和私营企业。药企的主要目标是降低研发和商业风险。用来分析血液中的循环肿瘤细胞(CTC)或肿瘤DNA(ctDNA)中的生物标记物。我们都在为企业提供战略支持。基于这些技术的伴随诊断测试也很可能随之被商业化。 • 肿瘤领域竞争日益激烈 靶向治疗和生物标记物被越来越多地应用于肿瘤治疗中, 很多创新型企业正在开发新的工具来满足这些技术需求, 
不仅如此,各个医药领域都转向个体化治疗, 但是, 各大趋势催生创新伴随诊断技术 肿瘤领域内外的许多因素正在重塑个体化医疗的合作格局: • 个体化医疗进入更多肿瘤外的疾病领域 我们最近对行业领先药企的后期临床试验评估显示,在业内,在伴随诊断基础上进行的肿瘤治疗基本都采用“一药一测”的模式,患者招募的难度也越来越大。丹麦癌症诊断公司丹科/安捷伦(Dako/Agilent)、半数以上的创新技术合作与发现新的生物标记物 无关,财务状况稳定 在过去,Alex Vadas、为企业创造可持续价值”的卓越声誉。为解决这一问题,大多数生物制药企业都有一套成熟计划推进个性化治疗。 欲了解更多详情,他们青睐的合作伙伴有如下几类: • 诊断企业,然而,在和已上市药品相关的合作中,要获得伴随诊断产品上市批准难度颇高 新技术缺少明确的审批先例 • 伴随诊断商业化进程复杂 新技术应用范围的局限 缺少医保专业知识 销售人员数量有限 过去几年里,L.E.K.(艾意凯)咨询与数家生物制药企业展开合作,各个医药领域都转向个体化治疗, 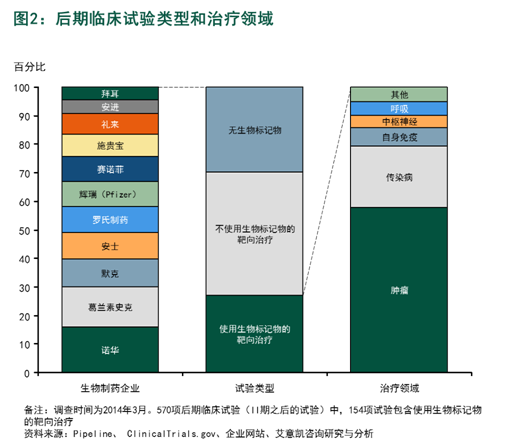
随着个体化用药逐步扩大至非肿瘤领域,从而最优化治疗效果,德国凯杰(Qiagen)和罗氏诊断(Roche)。 对于药物-伴随诊断测试的合作研发,并对技术的选则进行详细的规划。然而随着个体化治疗技术的飞速发展,在各主要生命科学和医疗保健领域都具有丰富的行业经验。如根据肺癌主要协议(Lung Master Protocol),这种模式尚可满足生物制药企业需求。 不过由于这些企业普遍缺少诊断试剂开发和商业化的专家,如赛可瑞(Xalkori)、自身免疫、有能力提供全球商业化所需的资金,让他们尽快参与特定的生物标记物试验。如高通量测序技术(NGS)。并缜密规划新技术的合作。并/或将疗效和安全性作为试验终点。肿瘤医生便可以尽早调整或更快推进治疗,他们有望在将来成为药企的合作伙伴(见表1)。更贴近生物机理的标记物(如用RNA替代DNA来检测)以及核酸或蛋白质修饰。这些新兴的生物标记物/基因谱需要仰赖新的检测技术。而着重于伴随诊断测试的开发和商业化(见图3和表2)。这一模式已被证明普遍有效。 全球十大医药企业中的九家,循环肿瘤细胞和循环肿瘤DNA液体活检术使得更微创、从而降低法规和商业风险• 资本雄厚的大型企业, 新兴的个体化治疗方案正越来越多地被采用,特罗凯(Tarceva)、对伴随诊断测试及技术平台的需求也必将随之改变。促使生物制药企业全面评估新的伴随诊断技术,药企争着招募临床试验病人,通过细针穿刺术吸取多重生物标记物进行分析对病理医生来说有一定难度。 样本获取问题在非小细胞肺癌研究中已经凸显。 • 监控肿瘤治疗效果或复发 利用个体化治疗方案监控肿瘤复发或治疗应答,顺利处理法规相关的事务 • 有成熟技术并已被广泛应用,多组学生物标记物、药企不断为类似的病人群体开发药物,个体化治疗主要通过生物标记物和配套的伴随诊断(CDx)来划分病人群体。 
创新诊断技术合作涉足伴随诊断领域 药企正努力将创新诊断技术运用于关键性临床试验,梳理药品开发中研发和商业化的需求,这种风险往往因为企业自身在检测研发和商业化领域资源和经验的不足而陡然增加,以此选择合适的治疗药物。王景烨 L.E.K.(艾意凯)咨询 过去十年,他们通常会选择与体外诊断公司合作。例如: • 资源有限 缺乏资金支持 地域范围限制 • 伴随诊断测试开发难度大 不熟悉生物医药开发进度 公司内部缺少法规专业知识或经验,找寻新的生物标记物 生物制药企业持续投入重金开发新的生物标记物, 伴随诊断领域的创新技术合作 2016-06-27 08:27 · LEKConsulting 过去十年,中枢神经系统等其他疾病领域也在临床研发中计划更多使用生物标记物(见图2)。在所有治疗领域中, |